Mit SMARTdrugs gegen Krebs
Jason Holland, Professor für Medizinische Radiochemie am Institut für Chemie, leitet das Forschungsprojekt «SMARTdrugs» an der UZH. «Unser Ziel ist es, supramolekulare Verbindungen zur Behandlung von zwei aggressiven Krebsarten zu entwickeln, die für betroffene Patientinnen und Patienten mit einer sehr schlechten Prognose verbunden sind: Lungen- und Hirntumore», sagt der Chemiker. Das vom Europäischen Innovationsrat (EIC) mit fast 4 Millionen Euro geförderte Projekt wird von fünf europäischen Teams umgesetzt, die komplementäre Fachkenntnisse und Technologien in synthetischer Chemie, radiopharmazeutischer Biologie sowie Krebsdiagnose und -therapie zusammenbringen.
Radionuklide in Krebsdiagnostik und -therapie
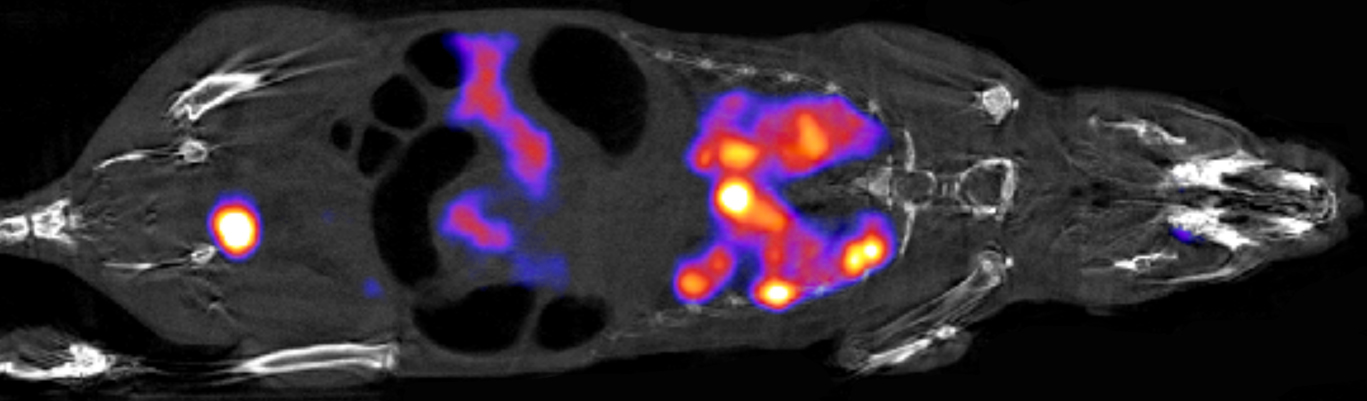
Für Onkologen ist es wichtig, die Grösse und Lage von Tumoren eines Patienten oder einer Patientin zu bestimmen. So können sie die beste Therapieoption wählen, die Behandlung über einen längeren Zeitraum verfolgen und deren Wirksamkeit prüfen. Tumore lassen sich mit Hilfe sogenannter Radiotracer sichtbar machen. Dabei handelt es sich um radioaktive Isotope eines chemischen Elements, die an ein Molekül gekoppelt sind, das die Krebszellen mit hoher Genauigkeit erkennt. Solche radioaktiven Wirkstoffe ermöglichen es den Klinikern, wichtige Tumorcharakteristika genau zu diagnostizieren. Die radioaktive Komponente erzeugt dabei Licht, das mit modernsten bildgebenden Verfahren wie der Positronen-Emissions-Tomographie (PET) nachgewiesen werden kann.
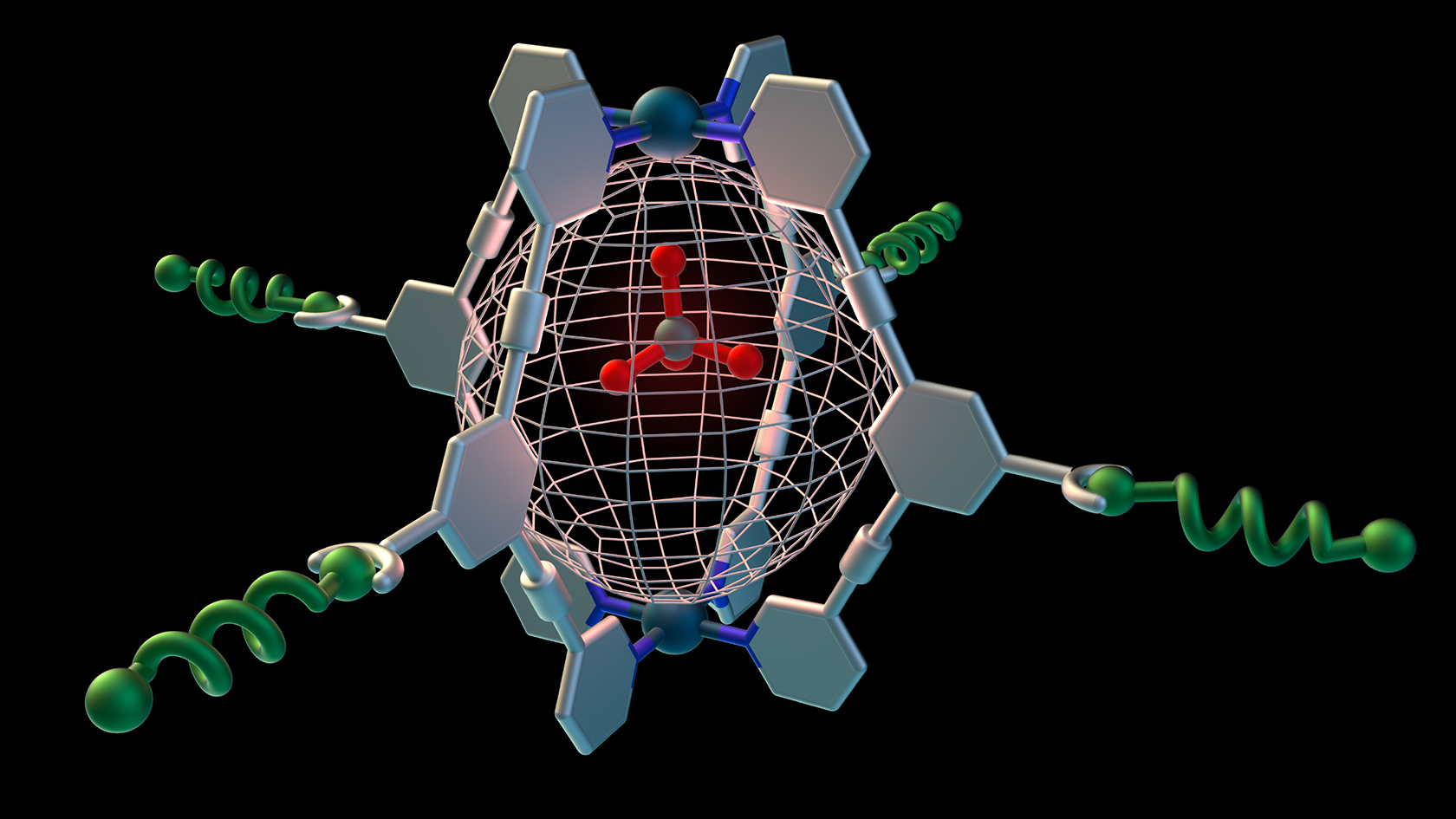
Radionuklide können auch zur Behandlung bestimmter Tumore eingesetzt werden. Hier wird das Radionuklid an ein Arzneimittelmolekül gekoppelt, das die kleine radioaktive Quelle gezielt an den gewünschten Ort lenkt. Durch die Anreicherung des therapeutischen Radiotracers im Tumor werden die Krebszellen abgetötet, während das umliegende gesunde Gewebe geschont wird. «Mit SMARTdrugs wollen wir eine neue Klasse von Therapien entwickeln: sogenannte Radiotheranostika. Dazu vereinen wir sowohl diagnostische als auch therapeutische Radionuklide in einem supramolekularen Wirkstoff», erklärt Holland. Anstatt Radionuklide direkt an Arzneimittelmoleküle zu binden, werden die Forschenden supramolekulare Verbindungen schaffen, deren Grösse, Form und weitere biochemischen Merkmale besser kontrolliert werden können als bei anderen sehr grossen Molekülen wie Proteinen. Diese Eigenschaften bestimmen, wie gut die neuen Verbindungen im menschlichen Gewebe wirken.

Unser Ziel ist es, supramolekulare Verbindungen zur Behandlung von zwei aggressiven Krebsarten zu entwickeln: Lungen- und Hirntumore
Neue Verknüpfungswege von Radionukliden
Die Grundlage für den Aufbau supramolekularer Radiotheranostika ist die synthetische Chemie. «Die Moleküle sind gross und sehr komplex. Sie werden mit Hilfe eines natürlichen Prozesses – der Selbstorganisation von Molekülen – entworfen und aufgebaut. Dabei addieren sich viele schwache Verbindungskräfte zu einem stabilen und gut definierten Arzneimittel», sagt Jason Holland. Vorbild dazu ist die Natur: In der Biologie wird die Selbstorganisation genutzt, um Proteine in ihre korrekte räumliche Form zu bringen. Diesen Prozess zu verstehen und für die Entwicklung wirksamer Medikamente zu nutzen, ist allerdings eine grosse Herausforderung.
Neuere Resultate der UZH und ihrer Kooperationspartner unter der Leitung von Angela Casini, Professorin für Medizinische und Bioanorganische Chemie an der Technischen Universität München in Deutschland haben bestätigt, dass neuartige therapeutische Moleküle mit Hilfe der Selbstorganisation hergestellt werden können. Parallel dazu hat das Team unter der Leitung von Jordi Llop, Experte für Radiochemie und nukleare Bildgebung am Center for Cooperative Research in Biomaterials im spanischen San Sebastian, gezeigt, dass radioaktive Nanoroboter Tumore effizient bekämpfen können. Diese nutzen chemische Brennstoffe, um ihre Ziele schneller zu finden.
Mit SMARTdrugs werden diese Ideen kombiniert und untersucht, wie die neuartigen Wirkstoffe die Therapie von Lungenkrebs und Hirntumoren verbessern können. Durchgeführt wird der klinische Teil des Projekts vom Team von Tim Witney, Spezialist für molekulare Bildgebung am britischen King's College London, und von der Gruppe von Alex Poot, Experte für Radiologie und Nuklearmedizin am Princess Maxima Hospital bzw. am University Medical Center im niederländischen Utrecht.
Bessere Therapien für Lungenkrebs und Hirntumore
SMARTdrugs konzentriert sich auf zwei aggressive Krebsarten: nicht-kleinzelliger Lungenkrebs bei Erwachsenen und Hirntumore bei Kindern. Die 5-Jahres-Überlebensraten liegen bei nur 15 bzw. 5 Prozent. Trotz Fortschritten in der Vorbeugung, Früherkennung und Behandlung hat sich die Medizin bei diesen Tumorarten in den letzten zehn Jahren nur wenig verbessert.
Lungenkrebs ist weltweit die häufigste krebsbedingte Todesursache und wird in verschiedene Subtypen eingeteilt. Der nicht-kleinzellige Lungenkrebs macht etwa 85 Prozent der Fälle aus. Auch zu den pädiatrischen Hirntumoren gehören mehrere Subtypen – etwa das Medulloblastom oder das diffuse Mittelliniengliom. Bei einigen davon beträgt die Lebenserwartung für Betroffene ab der Diagnose weniger als ein Jahr. Die derzeitigen Behandlungen scheitern oft an Tumorzellen, die durch Mutationen therapieresistent geworden sind.
«Radiotheranostika bieten grossartige Möglichkeiten zur Vorauswahl von Patienten, die am ehesten auf eine gezielte Therapie ansprechen, und zur Verbesserung der Behandlungsergebnisse. Das ermöglicht weitere Schritte in Richtung Präzisionsmedizin», betont Jason Holland. Doch bevor sie in klinischen Studien an Krebspatienten erprobt werden können, müssen die supramolekularen Radiotheranostika ihre Selektivität und Spezifität in zahlreichen Labortests unter Beweis stellen.