Haarnadel im Herzen des HI-Virus
Wo genau setzen Sie an, um die HI-Viren zu bekämpfen?
Nach einer HIV-Infektion dockt das Virus an die Wirtszelle an, verschmilzt mit dieser und schleust damit sein Erbmaterial aus dem Herzen des Virus in die Wirtszelle ein. Die Wirtszelle stellt dann Kopien her, wobei die Viren-RNA gelesen wird und nach deren Bauplan Virenproteine hergestellt werden. Schliesslich werden komplette Viren freigesetzt, diese können die nächsten Zellen befallen.
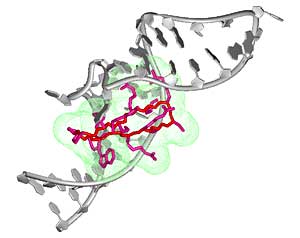
Ein wichtiger Schritt für die Steuerung der HIV-Vermehrung läuft im Kern der Wirtszelle ab: Nachgebaute Viren-RNA muss durch die Poren der Kernmembran in das Zytoplasma der infizierten Zelle transportiert werden, um dort in Proteine übersetzt oder in eine Virenhülle verpackt zu werden. Dieser Transport wird durch das sogenannte Rev-Virenprotein vermittelt, wobei eine argininreiche Domaine des Proteins an eine definierte Bindungsstelle der Viren-RNA, das sogenannte RRE-Erkennungselement, bindet.
Um diese Protein-RNA-Wechselwirkung (Rev-RRE) zu verhindern und damit das Ausschleusen der Virus-RNA aus dem Zellkern in das Zytoplasma zu stoppen, haben wir einen RRE-bindenden organischen Wirkstoff entwickelt. Unser «künstlich hergestellter» Inhibitor – ein zyklisches Haarnadel-Peptidmimetikum – ahmt die räumliche Struktur der alpha-helikalen Rev-Bindungsdomäne nach. Es brauchte eine Reihe von Optimierungs- und Screeningstufen, bis wir schliesslich ein Molekül entwickeln konnten, das fest und recht spezifisch an RRE bindet und in der Lage ist, das Rev-Protein aus den Rev-RRE-Komplexen zu verdrängen. Vereinfacht gesprochen wird damit die weitere Vermehrung des HI-Virus in den Zellen blockiert.
Wie unterscheidet sich Ihr Forschungsansatz von jenem anderer Gruppen, die ebenfalls versuchen, die Vermehrung der HI-Viren zu hemmen?
In unserem Designansatz wurden Moleküle entwickelt, die im Zellkern an die virale RNA binden, im Gegensatz zu Ansätzen, in denen virale Enzyme und Proteine als Zielmoleküle im Vordergrund stehen. Die beschriebene neue Klasse von Haarnadel-Peptidmimetika stellt damit einen Durchbruch auf der Suche nach wirkungsvollen RRE-Inhibitoren dar. Bisher hat man erfolglos danach gesucht.
Wie weit ist Ihre Forschung bereits gediehen?
Wir konnten zeigen, dass haarnadelähnliche Moleküle die Protein-RNA-Wechselwirkungen in viralen Zellen erfolgreich hemmen können. So konnte nachgewiesen werden, dass durch spezifische Wechselwirkungen mit der RNA-Bindungsregion ganz unterschiedliche HIV-1-Isolate, die alle wichtigen HIV-Untergruppen repräsentieren, gehemmt werden können.
Welches sind die nächsten Schritte?
Die aussichtsreichsten Kandidaten von Hemm-Molekülen werden für weiterführende präklinische Untersuchungen in Tiermodellen getestet. Wir wollen herausfinden, ob die Moleküle die gewünschte Wirkung im Organismus haben, und beziehungsweise oder ob mögliche unerwünschte Nebenwirkungen auftreten.