Die Genetik der Nachtblindheit

Tagsüber scheint alles in Ordnung. Wenn aber die Dämmerung anbricht, wird für nachtblinde Menschen die Welt noch dunkler als für Normalsehende. Die Konturen beginnen zu verschwinden, sichtbar sind nur noch einzelne helle Lichter, die Orientierung ist stark eingeschränkt. Schuld am eingeschränkten Sehvermögen sind die für das Sehen in der Nacht zuständigen Stäbchenzellen. Sie leiten im Falle der Nachtblindheit die optischen Signale nicht in Richtung Sehnerv weiter. Ausgelöst werden kann dies durch einen Mangel an Vitamin A in der Ernährung oder durch genetische Faktoren.
Forschungsgruppe aufbauen
Welche Gene dabei eine Rolle spielen, untersucht Dr. Christina Zeitz vom Institut für Medizinische Genetik in Schwerzenbach. Die studierte Chemikerin ist als Postdoktorandin am Lehrstuhl für Medizinische Molekulargenetik von Professor Wolfgang Berger tätig und baut derzeit eine Forschungsgruppe auf, welche sich spezifisch mit der Nachtblindheit beschäftigt. Dabei konnten die Zürcher Forschenden in Zusammenarbeit mit weiteren Forschungsgruppen im Oktober in einer Publikation im «American Journal of Human Genetics» neue Erkenntnisse vermelden.

Umweg über Mäuse
Bis vor wenigen Jahren waren fast ausschliesslich Fälle bekannt, bei denen Nachtblindheit über das X-Chromosom vererbt wurde. Das Forschungsteam um Christina Zeitz fand aber in der DNA von mehreren Betroffenen keine Mutationen auf dem X-Chromosom. Sie suchten daher in der Literatur nach Nachtblindheit bei Versuchstieren. Fündig wurden sie bei gentechnisch veränderten Mäusen, bei denen Forschende Nachtblindheit feststellten, sofern gewisse Gene «ausgeschaltet» wurden. Es handelte sich dabei um Gene auf so genannten «Autosomen», also demjenigen Teil des Erbgutes, der nicht zu den Geschlechtschromosomen gezählt wird.
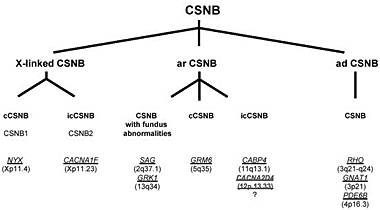
Die gesuchten Mutationen
Als Zeitz die DNA ihrer Patientinnen und Patienten auf Veränderungen in denselben Genen untersuchte, fand sie die gesuchten Mutationen. Das Gen «GRM6» hatte das Forschungsteam bereits 2005 beschrieben, mit «CABP4» haben sie nun in der neuen Publikation ein weiteres Gen identifiziert, über welches beim Vorliegen einer entsprechenden Mutation Nachtblindheit vererbt werden kann.
Das Krankheitsbild ähnelt zwar demjenigen bei einer Vererbung über das X-Chromosom, die Weitergabe der Krankheit verläuft aber unterschiedlich. Männliche Nachkommen haben ein Risiko von 50 Prozent an Nachtblindheit zu erkranken, wenn ihre Mutter eine Mutation auf dem X-Chromosom trägt. Weibliche Nachkommen erkranken nur in sehr seltenen Fällen, können die Mutation aber wiederum ihren Kindern weitergeben.
Mutationen in GRM6 und CABP4 werden immer autosomal rezessiv vererbt. Sind die Eltern Träger der Mutation, selber aber nicht erkrankt, besteht bei ihren Kindern eine Wahrscheinlichkeit von 25 Prozent, an Nachtblindheit zu erkranken.
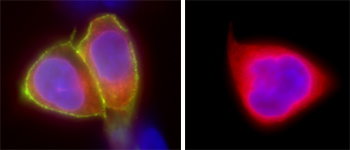
Verhinderter Botenstoff
Christina Zeitz hat auch erste Anhaltspunkte gefunden, wie diese Mutationen zum Ausbruch der Krankheit führen. Angelpunkt des Geschehens ist Glutamat, eine Aminosäure, die in der Netzhaut als Botenstoff wirkt. Zweierlei kann dabei schief gehen: Entweder kann das Glutamat wegen einer Veränderung in der Kalziumkonzentration die Stäbchenzellen nicht verlassen oder aber das Glutamat findet keinen Rezeptor, da dieser den Weg an die Zelloberfläche nicht geschafft hat.
Weitere Gene gesucht
Christina Zeitz vermutet, dass noch weitere Gene als Verursacher für Störungen bei der Weiterleitung der optischen Reize in Frage kommen: «Ich habe rund 50 Patienten, bei denen auch die jetzt bekannten Gene keine Erklärung für ihre Nachtblindheit liefern». Die Suche geht daher weiter, unterstützt durch Drittmittel und den Forschungskredit 2006 der Universität Zürich.
Die Resultate ihrer Forschung sind schon heute in der Diagnostik einsetzbar. Ärztinnen und Ärzte beispielsweise müssen die Nachtblindheit von der Retinitis Pigmentosa unterscheiden können. Auch diese Erkrankung der Netzhaut beginnt mit Nachtblindheit, kann aber zu gänzlicher Blindheit führen.
Neben der Verbesserung der Diagnostik will die Forschung am Lehrstuhl für Medizinische Molekulargenetik auch Grundlagen für bisher fehlende Therapiemöglichkeiten schaffen. Christina Zeitz: «Denkbar sind in Zukunft sowohl medikamentöse Behandlungen als auch Gentherapien. Um dieses langfristige Ziel zu erreichen, müssen wir aber zuerst die Entwicklung der Krankheit noch besser verstehen.»