Neue Erkenntnisse über Antibiotika-Resistenz
Infektionen durch Bakterien können mit Antibiotika erfolgreich bekämpft werden. Immer häufiger aber sind Bakterien resistent gegen Antibiotika und zwar nicht nur gegen eines, sondern gleich gegen mehrere. Eine Infektion, die von solchen resistenten Bakterien herrührt, kann nicht mehr bekämpft werden. Im schlimmsten Fall führt sie bei immungeschwächten Patientinnen und Patienten zum Tod.
Ein Forscherteam um Dr. Martin Pos und Markus Seeger vom Institut für Physiologie der Universität Zürich, sowie Dr. André Schiefner und Prof. Kay Diederichs von der Universität Konstanz haben nun den Bauplan einer Resistenz-Pumpe aufgedeckt, mit der bestimmte Bakterien Antibiotika bekämpfen: Mit einem einfachen Mechanismus pumpen sie schädliche Substanzen vom Innern des Bakteriums wieder hinaus.
Seltener Erfolg
Den Forschern an der Universität Zürich ist es gelungen, diese Membranpumpe zu isolieren und zu kristallisieren. «Die Kristallisation des Proteins war der schwierigste Teil, weil es selten gelingt, diese Art von Proteinen zu kristallisieren. Nach der Analyse der Kristalle durch die Forscher aus Konstanz konnte dann gemeinsam der Bauplan der Pumpe analysiert und daraus ihre Funktionsweise abgeleitet werden.» so Pos.
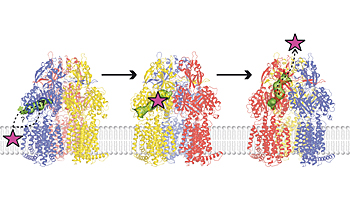
«Dem Bauplan nach beinhaltet die Pumpe ein Tunnelsystem, durch das die Antibiotika gleiten können», erklärt Martin Pos. Dieser Tunnel ist zuerst nur an einer zum Zellinnern gerichteten Seite geöffnet, um das Antibiotikum aus der Zelle zu fischen. Ist das Antibiotikum einmal im Tunnel gefangen, wird die innere Tunnelöffnung geschlossen, und gleichzeitig wird der Tunnel an der Aussenseite der Zelle geöffnet. Dadurch wird das Antibiotikum aus dem nach aussen geöffneten Tunnel gequetscht.
Ist das Antibiotikum einmal draussen und somit für das Bakterium ungefährlich, schliesst sich der Tunnel von aussen. Er öffnet sich wieder an der Innenseite, um sich das nächste Antibiotikum-Molekül zu angeln. Dieser Prozess wird ständig wiederholt und resultiert in einem kontinuierlichen Ausstrom von Antibiotika. Dies hat zur Folge, dass das Bakterium resistent ist und überlebt.
Den Tunnel verstopfen
Die Untersuchungen liefern Grundlagen für eine mögliche Bekämpfung der Antibiotika-Resistenz. «Mit den neuen Kenntnissen des Antibiotika-Pumpmechanismus ist es denkbar, einen Hemmstoff für diese Resistenz-Pumpe zu entwickeln» sagt Martin Pos. Denkbar sei ein Molekül, das sich an den engen Stellen des Tunnels verankert und diesen verstopft.